I batteri gengivali invadono le nostre cellule
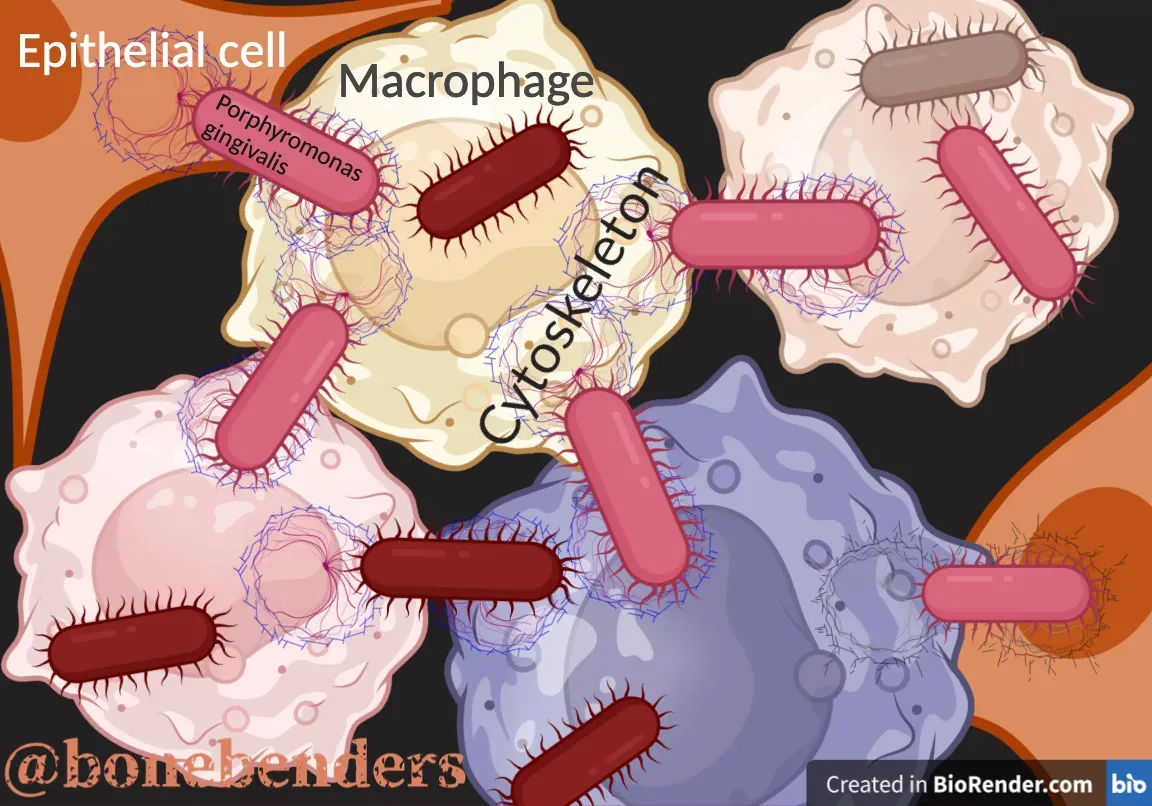
In breve — Porphyromonas gingivalis non resta nelle tasche parodontali. Invade le cellule ospiti, si trasmette da cellula a cellula attraverso ponti del citoscheletro e persiste in stato dormiente. Sfrutta CD47 e trombospondina-1 per evadere il sistema immunitario. Le sue gingipaine degradano proteine immunitarie chiave e possono alterare la barriera ematoencefalica. La persistenza intracellulare spiega le connessioni con Alzheimer, cancro gastrico e artrite reumatoide.
Summary (EN) — Porphyromonas gingivalis does not remain confined to periodontal pockets. It invades host cells, spreads cell-to-cell through cytoskeleton bridges, and persists in a dormant non-culturable state. It exploits CD47 and thrombospondin-1 to evade immune clearance. Its gingipains degrade key immune proteins and can disrupt the blood-brain barrier. This intracellular persistence explains connections with Alzheimer’s disease, gastric cancer, and rheumatoid arthritis.
Porphyromonas gingivalis vive nelle profondità delle tasche parodontali. Potrebbe sembrare una condizione statica. Non lo è.
Quando la malattia parodontale avanza, le specie aggressive prendono il sopravvento. P. gingivalis è tra queste. E ciò che fa è più simile a un’invasione militare che a una semplice infezione.
Il microambiente della tasca gengivale
La profondità della tasca gengivale è un luogo buio, caldo, scarsamente ossigenato. I batteri patogeni trovano rifugio anche nei depositi di tartaro che hanno contribuito a formare — una fortezza costruita con i propri mezzi.
Senza una terapia adeguata, queste specie si moltiplicano in modo esponenziale. Sono batteri Gram-negativi anaerobi: ottengono energia attraverso la fermentazione e la respirazione anaerobia, metabolizzando proteine e aminoacidi in assenza di ossigeno. I sottoprodotti — acidi grassi, idrogeno, metano, ammine — sono parte dell’arsenale chimico che aggredisce i tessuti circostanti.
L’invasione fisica
La grande massa microbica non si limita ad attaccare chimicamente con le tossine. P. gingivalis conduce una battaglia di prossimità.
Penetra fisicamente le cellule epiteliali della tasca gengivale, entrando nel citoplasma. Si muove da una cellula all’altra attraverso ponti del citoscheletro di actina. Prospera dentro le cellule ospiti — dalle epiteliali ai macrofagi, le sentinelle del sistema immunitario la cui funzione è precisamente digerire gli invasori.
L’arma è un enzima idrolitico che sopprime l’apoptosi ATP-dipendente. Una volta dentro il macrofago, P. gingivalis può disattivarne le armi e sopravvivere al suo interno. Ma questo è solo l’inizio.
I recettori di membrana
Il batterio si lega alle integrine β1 di membrana attraverso le fimbrie maggiori. Questo attiva FAK e paxillina, rimodellando il citoscheletro di actina per aprire la porta. L’invasione richiede la polimerizzazione dell’actina e la formazione di microtubuli. Dopo 24 ore si osserva un riassemblaggio significativo della rete filamentosa di actina e tubulina all’interno delle cellule dell’ospite.
In sostanza, il batterio utilizza le capacità contrattili del citoplasma delle cellule ospiti per spostarsi al loro interno.
Le vescicole di membrana esterna
P. gingivalis utilizza anche le vescicole di membrana esterna (OMV), ricche di gingipaine e fimbrie, per facilitare l’invasione cellulare. Queste vescicole entrano nelle cellule epiteliali tramite endocitosi con maggiore efficienza rispetto ai batteri interi. Una volta dentro, degradano le proteine epiteliali e facilitano l’adesione batterica.
Studi recenti hanno identificato oltre 300 proteine nelle OMV di P. gingivalis, tra cui gingipaine, fimbrie e peptidil-arginina deiminasi (PPAD), confermando il ruolo di queste vescicole come vettori di virulenza capaci di alterare il comportamento dei fibroblasti orali.
Come inganna il sistema immunitario
Qui la strategia si fa raffinata. P. gingivalis sfrutta la proteina CD47 della cellula ospite per evadere la risposta immunitaria. CD47 è il segnale “non mangiarmi” — lo stesso meccanismo che le cellule tumorali utilizzano per sfuggire alla sorveglianza immunitaria. L’attivazione di CD47 comunica al globulo bianco: “sono dei tuoi, lasciami stare”.
Quando CD47 viene bloccata con anticorpi neutralizzanti, la sopravvivenza intracellulare di P. gingivalis crolla drasticamente.
La proteina trombospondina-1 (TSP-1) collabora con CD47 nel reprimere l’attività battericida sia dei macrofagi che dei neutrofili. Un doppio scudo molecolare.
La degradazione delle difese immunitarie
Le gingipaine non si limitano a facilitare l’invasione. Degradano proteine immunitarie chiave dell’ospite: LL-37, un peptide antimicrobico capace di legare l’amiloide-beta e bloccarne l’aggregazione; l’apolipoproteina E; gli interferoni antivirali. Questa azione sistematica di demolizione indebolisce l’immunità innata e crea le condizioni per infezioni persistenti.
Sopravvive all’interno delle nostre cellule
P. gingivalis non si limita a invadere. Persiste nelle cellule in uno stato dormiente — non coltivabile in laboratorio ma vivo, rilevabile. Questo spiega perché le infezioni parodontali sono così difficili da eradicare: il batterio si nasconde dove gli antibiotici non arrivano efficacemente.
Le conseguenze superano i confini della bocca. P. gingivalis è stato trovato nel tessuto aterosclerotico, nel cervello di pazienti con Alzheimer, ed è associato a rischi durante la gravidanza, cancro gastrico e artrite reumatoide.
L’asse bocca-intestino-cervello
Ricerche recenti hanno dimostrato che l’infezione orale da P. gingivalis altera il microbiota intestinale, compromette la barriera intestinale e attiva risposte infiammatorie sistemiche. In particolare, il batterio altera il metabolismo del triptofano attraverso la via della chinurenina, producendo metaboliti neurotossici come la 3-idrossichinurenina che inducono apoptosi neuronale. Un percorso che collega la tasca parodontale al cervello passando dall’intestino.
Le gingipaine, inoltre, possono compromettere la barriera ematoencefalica, consentendo il trasporto di fattori di virulenza — incluse le vescicole di membrana esterna — direttamente al tessuto cerebrale, dove innescano neuroinfiammazione e promuovono l’accumulo di amiloide-beta e l’iperfosforilazione della proteina tau.
La battaglia contro questo batterio non è una questione di igiene. È una guerra cellulare dove il nemico usa strategie di guerriglia molecolare, nascondendosi dentro le nostre stesse cellule, sovvertendo le nostre difese e, da lì, raggiungendo organi distanti attraverso percorsi che stiamo appena iniziando a comprendere.
Articoli per approfondire
Immagine di copertina creata con biorender.
FAQ
Qual è il ruolo di Porphyromonas gingivalis nelle tasche parodontali?
Porphyromonas gingivalis colonizza le profondità delle tasche parodontali, dove si moltiplica in modo aggressivo sfruttando un ambiente anaerobio, contribuendo alla progressione della malattia parodontale.
In che modo P. gingivalis si adatta all’ambiente della tasca gengivale?
Il batterio prospera in un ambiente buio e privo di ossigeno, ottenendo energia tramite fermentazione e respirazione anaerobia, metabolizzando proteine e aminoacidi e producendo composti come acidi grassi, gas e ammine.
Come invade P. gingivalis le cellule dell’ospite?
P. gingivalis penetra fisicamente le cellule epiteliali legandosi alle integrine β1 tramite fimbrie, rimodellando il citoscheletro di actina. Si trasmette da cellula a cellula attraverso ponti citoscheletrici e utilizza vescicole di membrana esterna cariche di gingipaine per facilitare l’invasione.
Come evade il sistema immunitario?
Il batterio sfrutta la proteina CD47 dell’ospite come segnale “non mangiarmi”, collaborando con la trombospondina-1 per sopprimere l’attività battericida di macrofagi e neutrofili. Le gingipaine degradano inoltre proteine immunitarie chiave come LL-37 e interferoni.
Perché è difficile eliminare definitivamente P. gingivalis?
Il batterio persiste nelle cellule in uno stato dormiente, non coltivabile ma ancora vivo. Si nasconde dove gli antibiotici arrivano con difficoltà. Questa persistenza intracellulare spiega anche le connessioni con malattie sistemiche come l’Alzheimer.
Cerchi uno specialista?
Parodontologia a Frosinone →Diagnosi e trattamento della parodontite nello Studio Denti Più
Hai bisogno di un parere?
Prenota una visita nello studio del Dr. Bruschi a Frosinone. Prima visita con diagnosi completa e piano di trattamento personalizzato.
Resta aggiornato
Nuovi articoli su parodontologia, implantologia e chirurgia orale — nella tua casella email.
Commenti
Caricamento commenti...
Lascia un commento